Криоабляция рака молочной железы
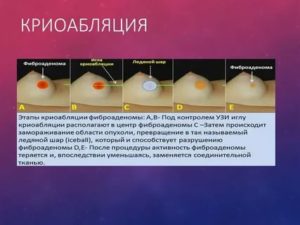
Криоабляция фиброаденомы молочной железы
Обнаружить опухоль женщина может при самообследовании, врач-маммолог определяет патологическое уплотнение во время пальпационного осмотра. Для верификации диагноза и разработки плана лечения специалисты назначают следующие диагностические процедуры:
- общий и биохимический анализ крови и мочи;
- маммография;
- УЗ-исследование молочной железы.
Данные методы обследования позволяют выяснить общее состояние организма, определить локализацию, размер, форму опухоли. Также врачи проводят процедуру пункционной биопсии, чтобы выяснить морфоцитологическую структуру фиброаденомы и исключить наличие злокачественных клеток.
Стоимость лечения
Качество лечения в московских клиниках сегодня ничем не уступает уровню медицинских услуг ведущих медцентров мира, о чем свидетельствуют многочисленные отзывы пациенток и статистические показатели результатов.
Общая стоимость полного курса лечения фиброаденомы молочной железы рассчитывается индивидуально, в зависимости от применяемых лечебно-диагностических методов, квалификации врачей, срока пребывания в стационаре и других факторов.
Преимущества платного лечения
Платное лечение фиброаденомы молочной железы в клиниках Москвы отличается такими преимуществами:
- штат опытных маммологов, хирургов и специалистов других меднаправлений;
- применение щадящих хирургических методов, которые при необходимости сопровождаются пластической коррекцией с отличным эстетическим результатом;
- использование новейшего медоборудования;
- комфортные палаты, внимательное отношение медперсонала.
Если вам необходимо лечение фиброаденомы молочной железы в одной из московских клиник, оставьте заявку на сайте или позвоните по телефону горячей линии. Мы проконсультируем вас по всем вопросам и поможем госпитализироваться в любой медцентр столицы в кратчайшие сроки.
Как лечить фиброаденому молочной железы
По сути, методов лечения всего два: оперативный и консервативный. Причём, оперативный метод преобладает, так как лечение без операции приводит к рассасыванию фиброаденомы только в 10% случаев.
- Размер образования в груди больше 2 см,
- Когда за несколько месяцев фиброаденома увеличилась в 2-3 раза,
- При подозрениях на онкологию.
Операция при фиброаденоме может быть разных видов:
- Секторальная резекция,
- Тотальная резекция,
- Энуклеация (вылущивание).
Основная причина фиброаденомы — гормональный дисбаланс.
При секторальной резекции удаляется часть молочной железы с опухолью.
Тотальная резекция в случае фиброаденоматоза проводится редко. В ходе тотальной резекции удаляется вся молочная железа. Это бывает необходимо при озлокачествлении процесса при листовидной фиброаденоме.
При энуклеации удаляется только опухоль, а ткани груди полностью сохраняются.
В зависимости от вида операции, особенностей и желания пациентки она может проводиться под общим наркозом или под местной анестезией. В среднем продолжительность её около часа.
После операции назначается гормональная терапия для нормализации фона гормонов, ведь именно их дисбаланс и становится основной причиной развития фиброаденомы.
- Динамическое наблюдение,
- Гормональная терапия,
- Криотерапия,
- Лазерная абляция,
- Радиочастотная терапия,
- Гомеопатическое лечение.
Конечно, большинство женщин хотели бы выбрать консервативное лечение фиброаденомы молочной железы без операции, но это не всегда возможно. Рассмотрим эти методы несколько подробнее.
Методы консервативной терапии
Лечение фиброаденомы грудины у женщин направлено на нормализацию гормонального фона, избавление от лишнего веса и сопутствующих болезней мочеполовых органов.
Чтобы подобрать медикаментозный курс терапии, необходимо определить вид опухоли. Узелковая форма не трансформируется в злокачественную.
По месту расположения она делится на три подвида – интраканаликулярная, периканаликулярная и смешанная.
Листовидная форма встречается редко. Этот опасный вид часто превращается в саркому. Имеет неровные контуры, неоднородную структуру, отсутствие капсулы, стремительный рост. Показано хирургическое вмешательство.
Если опухоль маленькая, назначают средство Прожестожель. Гель наносят на кожу груди 2 раза в день. Лекарство не попадает в систему кровообращения и считается относительно безопасным.
Дюфастон снижает концентрацию эстрогена, что способствует рассасыванию опухоли или приостанавливает ее рост.
Гомеопатия и БАДы
Это вспомогательный метод борьбы. Препараты растительного происхождения не дают возможность избавляться от узлов в груди, они стабилизируют гормональный фон, укрепляют иммунитет, облегчают симптомы и улучшают общее самочувствие. Их действие наступает медленнее, чем от синтетических препаратов.
Капли или таблетки Мастодиона снижают уровень пролактина. Их назначают, если опухоль не имеет капсулы и четких контуров.
При дефиците йода в организме добавляют йодсодержащие препараты.
Также используется гирудотерапия. Эффект от процедуры связан с тем, что пиявки могут выделять биологически активные вещества.
Витаминотерапия
Народные средства не способны вылечить фиброаденому
Особая роль отводится витаминному комплексу. Витамин Е регулирует обменные процессы в организме, активизирует действие прогестерона. За понижение пролактина отвечает фолиевая кислота и витамин B6. Для укрепления стенок сосудов, снижения отеков добавляют витамины C, P и PP.
Народные средства
Средства народной медицины не могут вылечивать фиброаденому. Их используют как дополнение к комплексной терапии.
Рекомендуются солевые аппликации. Чайную ложку соли растворяют в 200 мл теплой воды. Ткань пропитывают раствором и прикладывают на участок грудины, где есть образование. Процедуру лучше делать на ночь.
Лист капусты смазывают медом и прикладывают к больной груди на 12 часов. В случае аллергии мед можно заменить растопленным маслом и посыпать слегка солью.
При фиброаденоме для приема внутрь используют лекарственные растения: кору дуба, корень алтея, фенхеля и солодки, кожуру граната, цветки ромашки. Изготовленные настои и отвары стимулируют иммунитет, стабилизируют гормоны. Вербену применяют как наружное средство. Ткань, смоченную отваром, прикладывают к больному месту.
Помогает уменьшить опухоль мазь. Ее готовят из муки, перемешанной с медом: 1 столовая ложка меда и 2 муки. Полученным составом смазывают грудь утром и вечером.Следующее средство изготавливают из 1 стакана растительного масла. Его разогревают и добавляют большой кусок воска. После растворения вводят сваренное, измельченное куриное яйцо. Выдерживают состав на водяной бане 30 минут. Мазь втирают в пораженное место на протяжении 2–3 недель. После недельного перерыва курс повторяют.
Учитывая токсичность растения, официальная медицина не использует чистотел. Однако по отзывам о лечении фиброаденомы молочной железы без операции, препарат приостанавливает разрастание опухоли, укрепляет иммунитет, устраняет очаги воспаления, снимает боль.
Тактика лечения зависит от характеристик фиброаденомы и возраста пациентки. При опухоли небольшого размера (до 8-9 мм) девушки или женщины находятся под пристальным наблюдением врачей и 1 раз в несколько месяцев проходят процедуру УЗИ молочной железы.
Консервативная терапия включает контроль над динамикой течения болезни, коррекцию гормонального фона, устранение гинекологических проблем и лечение сопутствующих заболеваний.
Но как показывает практика, даже при комплексном консервативном подходе фиброаденома молочной железы рассасывается крайне редко.
Показания к оперативному вмешательству: прогрессивный рост фиброаденомы филлоидного типа (до 4-5 см за несколько месяцев), планирование беременности, физический и психологический дискомфорт, вызванный косметическим дефектом (деформацией молочной железы) при крупных опухолях. Хирургическое лечение проводится под местным или общим наркозом с помощью таких методов:
- Секторальное удаление — иссечение опухолевого образования вместе с окружающими тканями молочной железы с захватом от 1 см. Проводится в случае подозрений на озлокачествление фиброаденомы.
- Энуклеация — малоинвазивное лапароскопическое вылущивание опухоли, исключающее постоперационные осложнения. После энуклеации проводят гистологический анализ удаленных тканей.
За счет качественных разрезов и наложения подкожных швов, хирурги достигают хорошего косметического эффекта. Операция противопоказана при тяжелых заболеваниях крови, почек, сердечнососудистой и дыхательной системы.
Лазерная абляция — безопасное лечение фиброаденомы размером до 3 см с помощью лазера, который разрушает уплотнение без изменений формы молочной железы. Процедура проводится под местной анестезией и не требует реабилитации. После лазерной абляции на месте устраненной опухоли спустя 60-80 дней восстанавливается соединительная ткань.
Криоабляция — высокоточное замораживание фиброаденомы низкотемпературным жидким азотом через прокол криозонда под ультразвуковым контролем. Метод используется при множественных или единичных образованиях диаметром до 3,5-4 см.
Радиоволны — редко применяемая методика лечения, эффективная на ранней стадии патологии. В процессе радиоволновой операции рассекают ткани и уничтожают опухолевые клетки направленным высокочастотным радиоизлучением.
Маммотомическая биопсия — миниинвазивное удаление фиброаденомы. Во время процедуры используют биопсийный зонд, через который вакуумом эвакуируют пораженные ткани молочной железы.
Нехирургическое лечение
Динамическое наблюдение предполагает регулярный УЗИ-контроль состояния опухоли.
Если размеры узла не более 2 см и он женщину не беспокоит, тенденций к росту нет, то применяется такой метод.
Гормональное лечение назначают при таких же размерах опухоли, однако очень часто после окончания лечения размеры фиброаденоматоза молочной железы снова увеличиваются.
Лечение гомеопатией
Гомеопатическое лечение фиброаденомы молочной железы в основном используется в качестве вспомогательного средства.
Препараты на основе трав для внутреннего и наружного применения снимают боли в груди и облегчают симптомы, возникающие в конце менструального цикла.
Лечение фиброаденомы народными средствами
:
- Взять 2 ст. л. вахты и мяты, добавить по ложке корня валерианы и шишек хмеля, тщательно размешать, затем 1 ст. л. смеси залить стаканом кипяченой воды и настоять 30 минут. Принимать настой по полстакана три раза в день до еды.
- Взять 3 ч. л. травы полыни, залить стаканом кипятка и настоять два-три часа. Принимать по чайной ложке после завтрака и обеда. С третьего дня лечения дозировку увеличить до столовой ложки. Курс лечения: 10 дней.
- При фиброаденоме народное лечение можно проводить и с помощью обычного картофеля. Рецепт: приготовить полстакана сока свежего картофеля (картофель перетереть и отжать через марлю) и выпить его за 20 минут до еды. Принимать картофельный сок три раза в день на протяжении трех недель.
Как получить квоту на лечение фиброаденомы молочной железы
Оформление квоты на высокотехнологичную медицинскую помощь — длительный и сложный процесс. Пациенты проходят массу обследований и собирают большой пакет документов для одобрения бюджетного финансирования в трех медкомиссиях: там, где планируется лечение фиброаденомы молочной железы, в больнице по месту прописки и областном департаменте здравоохранения.
Сколько стоит лечение
Оценить полную стоимость лечения фиброаденомы молочной железы заочно невозможно, так как она зависит от объёма диагностических и лечебных процедур. Если выполняется оперативное лечение, то может понадобиться дополнительное пребывание в стационаре, которое существенно увеличит стоимость всего лечения.
Лучшие клиники по лечению фиброаденомы в Израиле и Германии.
Предсказать «поведение» организма не всегда возможно. По этим причинам даже в ответ на запрос пациентки с предоставлением предварительных диагнозов клиника представляет информацию лишь о предварительной цене.
Чаще всего за лечением фиброаденомы молочной железы пациентки обращаются в клиники Израиля и Германии.
Израиль
Ведущие клиники Израиля Ассута и Ихилов оснащены самым современным оборудованием и в состоянии проводить лечение любыми современными и традиционными методами.
Стоимость лечения может составлять от 2000 $.
Германия
В Германии большинство университетских клиник многопрофильные и предлагают услуги по лечению фиброаденомы.
Например, Клиника гинекологии и родовспоможения в городе Аахен, Клиника оперативной гинекологии в Мёнхенгладбахе, Университетская клиника Мюнхена.
Средняя стоимость такого лечения в Германии составляет 2000-5000 €.
Россия
В российских клиниках тоже можно пройти лечение фиброаденомы. Лазерные или радиочастотные технологии нельзя пока назвать освоенным нашими врачами.
Хирургическое же лечение выполняется на хорошем уровне, стоимость операции в среднем 20000 рублей. В некоторых клиниках могут провести лечение за 8000 рублей, а могут и за 35000-40000 рублей.
Дополнительную информацию смотрите в разделе Онкология.
Источник: https://zdorov4ik.ru/krioablyatsiya-fibroadenomy-molochnoy-zhelezy/
Чрескожная криоабляция фиброаденомы молочной железы | Шачинов Е.Г., Балахнин П.В., Шмелев А.С., Малькевич В.И., Бит-Сава Е.М., Егоренков В.В., Моисеенко В.М
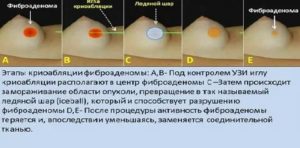
Чрескожная криоабляция фиброаденомы молочной железы
Фиброаденома (ФА) — наиболее часто встречающаяся доброкачественная опухоль молочной железы (МЖ) у женщин репродуктивного возраста [1]. ФА чаще всего обнаруживается в возрасте до 35 лет, но может быть выявлена и позднее при профилактическом обследовании [2].
Опухоль состоит из фиброзной и железистой ткани в различных пропорциях и, как правило, имеет капсулу и четкие границы. Часто заболевание протекает бессимптомно и требует только динамического наблюдения. Однако наличие ФА может вызывать определенное беспокойство у женщин, приводящее к желанию избавиться от новообразования.
Показаниями к оперативному лечению (хирургическое удаление или вакуумная аспирационная экстракция опухоли) являются быстрый рост ФА, атипичный вид опухоли при ультразвуковом исследовании (УЗИ), а также наличие симптомов и активное желание самой пациентки [3].
Хирургическое вмешательство — это инвазивный метод лечения, требующий выполнения разреза и нередко приводящий к формированю рубца как на поверхности кожи, так и в ложе опухоли. При удалении крупных новообразований также возможно появление деформации (дефекта/западения) контуров МЖ [1].
Вакуумная экстракция считается менее инвазивным вариантом терапии, однако при ее проведении часто не удается достичь полного (радикального) удаления всей опухолевой ткани, в связи с чем возможен повторный рост ФА [4].
Впервые замораживание как метод лечения опухолей МЖ описал еще в 1851 г. James Arnott, который для этих целей использовал охлажденный до очень низких температур (около -20 °С) гипертонический солевой раствор со льдом [5]. В 1960-е гг.
были созданы первые экспериментальные криогенные установки, работавшие на жидком азоте. Первая коммерчески доступная система (второго поколения), основанная на методе накачки жидкого азота, была выпущена в 1991 г., однако существенным недостатком данной системы являлся очень большой диаметр криозондов (1 см и более).Стремительное развитие чрескожной криоабляции (ЧК) в последнее десятилетие связано с созданием в начале 2000-х гг. аргоно-гелиевых криогенных установок третьего поколения, в которых для охлаждения криозондов используется не жидкий азот, а находящийся под большим давлением аргон [5].
Изменение технологии охлаждения криозондов позволило уменьшить их диаметр до размеров обычной биопсийной иглы (17 G, или 1,5 мм), что сделало возможным безопасное использование ЧК для лечения различных новообразований [6–8].
В настоящее время ЧК под УЗ-контролем рассматривается как один из наиболее перспективных минимально инвазивных методов лечения ФА МЖ [9–11].
Преимуществами ЧК перед другими видами радикальной терапии ФА являются безболезненность, атравматичность, надежный мониторинг выполнения процедуры (путем визуализации ледяного шара), а также отсутствие рубцов на коже в месте вмешательства [2, 9–11]. Однако в отечественной литературе сведения о технических особенностях проведения ЧК ФА МЖ, а также о ее результатах в настоящее время практически отсутствуют.
Цель исследования — в рамках проспективного исследования изучить технические аспекты, а также непосредственные и ближайшие результаты применения ЧК под УЗ-контролем в лечении ФА МЖ диаметром до 30 мм на большой группе пациенток.
Материал и методы
В проспективное исследование были включены 29 пациенток с морфологически верифицированной одиночной ФА МЖ, которым с января 2016 г. по декабрь 2017 г. выполнили ЧК ФА МЖ. Возраст пациенток на момент операции составлял 22–51 год (в среднем — 32,2±1,17 года, медиана — 30,5 года).
Критериями включения в исследование были наличие отчетливо визуализируемой при УЗИ одиночной ФА диаметром ≤30 мм, характеризующейся ростом в течение последних 6 мес., а также желание пациентки. Размер ФА в наибольшем измерении (по длинной оси) варьировал от 13 до 30 мм, в среднем — 21,0±0,99 мм, медиана — 20,0 мм.
Процедуры криоабляции выполняли хирурги отделения рентгенохирургических методов диагностики и лечения (ОРХМДиЛ), имеющие стаж работы по специальности более 15 лет.
Все врачи имели опыт использования чрескожной энергетической абляции (радиочастотной абляции, микроволновой абляции и криоабляции) для лечения первичных и метастатических опухолей различных локализаций более чем у 200 пациентов.
Кроме того, все хирурги прошли дополнительное обучение по методике проведения ЧК ФА МЖ в соответствии с международной образовательной программой компании Galil Medical (США).
До начала процедуры с целью планирования вмешательства осуществляли тщательный осмотр пациенток, пальпацию и УЗИ МЖ. УЗИ выполняли на ультразвуковой диагностической системе Vivid I (GE HealthCare, США) линейным датчиком 8L RS (4,0–13,0 МГц).Полученные данные использовали для составления плана проведения ЧК в зависимости от объема МЖ, размеров и локализации ФА.
При этом заранее определяли точку введения криозонда, траекторию таргетирования опухоли, длительность и интенсивность замораживания, а также возможность применения дополнительных манипуляций для защиты кожи и плевры от термического повреждения. У всех пациенток на проведение ЧК было получено добровольное письменное информированное согласие.
Во всех случаях процедуру абляции проводили амбулаторно в рентгеноперационной ОРХМДиЛ на аргоно-гелиевой криогенной установке SeedNet Gold (Galil Medical, США) с использованием криозонда IceSphereTM (Galil Medical, США) диаметром 17 G, или 1,5 мм (рис. 1).
Первым этапом вмешательства под УЗ-контролем выполняли местную анестезию места пункции 20 мл 1% раствора лидокаина. После этого проверяли работоспособность криозонда in vitro путем погружения его рабочей части в физиологический раствор и включения криогенной установки в тестовом режиме (рис. 2 А).
Точку входа криозонда на коже располагали по передней подмышечной линии или по маммарной складке. Также с целью обеспечения косметического эффекта введение криозонда в кожу производили только путем ее прокола, без использования дополнительного разреза. После этого под контролем УЗ осуществляли установку аппликатора в опухоль.
При этом позиционирование криозонда выполняли таким образом, чтобы он проходил через центральную ось ФА по ее максимальному длиннику, а центр будущего ледяного шара (формируется в 12 мм от кончика аппликатора) располагался в центре опухоли (рис. 3 А, Б).
После контрольного сканирования в разных проекциях и под разными углами озвучивания убеждались в том, что положение криозонда в опухоли адекватное, и начинали процесс ЧК.
Криоабляцию осуществляли в 100% режиме подачи аргона при постоянном мониторинге формирования ледяного шара с помощью УЗИ в режиме реального времени (рис. 2 Б, рис. 3 В). Замораживание выполняли до тех пор, пока границы ледяного шара не выходили за границы опухоли как минимум на 3 мм по всей ее поверхности.Таким образом, при правильно проведенной процедуре ЧК размеры зоны абляции должны были превышать размеры ФА не менее чем на 6 мм. При близком предлежании опухоли к коже (менее 3 мм) для предотвращения ее термического повреждения (промораживания) к МЖ в зоне ЧК прикладывали стерильную хирургическую перчатку, наполненную горячим физиологическим раствором.
При локализации опухоли недалеко от плевры использовали гидродиссекцию, заключавшуюся во введении 20–40 мл стерильного физиологического раствора в клетчатку МЖ между ФА и легким, что давало возможность отодвинуть опухоль и выполнить процедуру без термического повреждения плевры. После достижения целевых размеров ледяного шара подачу аргона прекращали и дожидались пассивного (т. е.
без использования гелия) оттаивания всей зоны абляции, которое занимало 10–12 мин и мониторировалось с помощью УЗИ. Далее проводили второй цикл криоабляции (цикл замораживания — оттаивания) по аналогичной схеме, удаляли криозонд и выполняли механическую компрессию МЖ в течение 10–15 мин.
После окончания процедуры на МЖ накладывали давящий бандаж и в течение 3 ч наблюдали пациентку в палате дневного пребывания. Дальнейшее динамическое наблюдение осуществляли по данным контрольных осмотров и результатов УЗИ, которые выполняли через 3, 6 и 12 мес. после вмешательства.
В рамках исследования проспективно анализировали технический успех (и техническую эффективность) процедуры ЧК, число и виды осложнений, динамику уменьшения размеров (объема) зоны абляции, состояние кожи в месте входа (вкола) криозонда, а также общую удовлетворенность пациенток выполненным вмешательством.
Результаты исследования
За период с января 2016 г. по декабрь 2017 г. 29 пациенткам проведено 29 сеансов ЧК. Все проведенные процедуры ЧК были расценены как технически успешные (выполнен запланированный объем вмешательства) и технически эффективные — во всех случаях удалось достичь перекрытия опухоли ледяным шаром не менее чем на 3 мм от поверхности.
Длительность замораживания (подачи аргона), потребовавшаяся для достижения целевых параметров абляции, варьировала от 4 до 14 мин в зависимости от размеров ФА и в среднем составила 7 мин 6 с ± 30 с (медиана — 6 мин 30 с).
У 2 пациенток с близким расположением опухоли возле плевры потребовалось выполнение гидродиссекции для предотвращения термического повреждения последней.В 3 случаях в связи с поверхностной локализацией ФА для исключения промораживания кожи на время криоабляции к МЖ прикладывали стерильную хирургическую перчатку, заполненную горячим физиологическим раствором. Еще в 1 случае подкожного расположения опухоли потребовалось применение комбинированной методики в виде гидродиссекции и прогревания кожи.
В первые 3 сут после ЧК все пациентки отмечали минимальный дискомфорт, болезненность и отечность МЖ на стороне вмешательства, не требовавшие применения лекарственных препаратов.
Только в 3 случаях (10,3%) после ЧК возникли умеренные боли в МЖ, сопровождавшиеся развитием гематомы в месте пункции и в месте выполненной абляции (рис. 4 А, Б). Боли были купированы в течение 1 сут после процедуры приемом нестероидных противовоспалительных препаратов.
Гематомы исчезли самостоятельно в течение 2 нед. после вмешательства и не потребовали лекарственного или хирургического лечения.
Уменьшение размеров зоны абляции в течение первого года после ЧК наблюдалось у 26 пациенток, что составило 89,7% случаев (рис. 4 В, Г). При этом по данным УЗИ объем зоны абляции уменьшился в среднем на 28%, 54% и 70% через 3, 6 и 12 мес. наблюдения соответственно.
У 3 пациенток (10,3%) зона абляции не имела тенденции к уменьшению размеров, однако случаев ее увеличения или повторного появления ФА за период наблюдения отмечено не было. Только у 6 пациенток (20,7%) через 12 мес.
после ЧК в МЖ пальпировалось резидуальное образование, соответствующее зоне выполненной абляции. До выполнения ЧК 9 пациенток (31,0%)жаловались на периодические ноющие боли в МЖ на стороне образования. Через 12 мес.
после операции боли сохранялись только в 2 наблюдениях (6,9%), при этом интенсивность их существенно снизилась.
В процессе наблюдения не было выявлено ни одного случая появления рубцовой ткани на коже в месте входа (вкола) аппликатора. Через 1 год после вмешательства только у 2 пациенток (6,9%) в месте вкола на коже определялись минимальные изменения (неравномерная пигментация), в то время как в остальных случаях какие-либо следы выполненного вмешательства полностью отсутствовали.Удовлетворенность пациенток результатами лечения (как косметическим, так и терапевтическим эффектом) через 3, 6 и 12 мес. после процедуры ЧК составила 93,1% (n=27), 93,1% (n=27) и 89,7% (n=26) соответственно.
Обсуждение
В проведенном нами исследовании у 26 из 29 пациенток (89,7%) после выполнения ЧК отмечено прогрессивное уменьшение размеров зоны абляции в течение первых 12 мес. наблюдения. Известно, что скорость и выраженность регресса зоны абляции зависят главным образом от соотношения железистой и фиброзной ткани, содержащейся в ФА [9].
Как было показано ранее, опухоли, состоящие преимущественно из железистой ткани, после ЧК подвергаются значительно более быстрой инволюции, чем ФА с высокой долей соединительнотканных волокон [9–11]. При этом уменьшение размеров зоны абляции происходит не только в первый год после процедуры ЧК, но и продолжается в течение следующих 12 мес. [2, 3, 9, 10].
Это позволяет надеяться на еще большее уменьшение объема зон абляции у наших пациенток в дальнейшем.
Высокая удовлетворенность пациенток результатами лечения в нашем исследовании была связана не только с хорошим терапевтическим, но и с очень хорошим косметическим эффектом, наблюдавшимся даже несмотря на то, что большинство образований было достаточно большого диаметра (в среднем — 21 мм).
Связано это с тем, что после ЧК девитализированная ФА естественным образом реабсорбируется организмом и замещается здоровыми тканями. В связи с этим после ЧК не возникает деформации (дефекта/западения) контуров МЖ, даже в случаях лечения крупных новообразований [2, 9].
Кроме того, благодаря отсутствию разрезов на коже практически не остается никаких следов от выполненного вмешательства [10, 11].
ЧК обладает рядом неоспоримых преимуществ перед гипертермическими видами энергетического воздействия — радиочастотной, микроволновой и лазерной абляцией [6, 7]. Во-первых, проведение ЧК абсолютно безболезненно, в связи с чем не требует наркоза.
Во-вторых, благодаря визуализации ледяного шара с помощью УЗИ возможен постоянный мониторинг процедуры, существенно повышающий ее прецизионность.В-третьих, в зоне абляции после ЧК не остается грубого рубца, значительно затрудняющего УЗИ- и МРТ-визуализацию МЖ в том случае, если пациентке необходимо дальнейшее динамическое наблюдение [10, 11].
Заключение
Таким образом, проведенное нами исследование показало, что ЧК под УЗ-контролем может рассматриваться как метод выбора для лечения ФА МЖ диаметром ≤30 мм.
ЧК является наиболее перспективным минимально инвазивным, эффективным и безопасным методом терапии, сопровождающимся высокой удовлетворенностью пациенток косметическим и терапевтическим результатами вмешательства, что связано с возможностью выполнения операции в амбулаторном режиме, непродолжительным временем вмешательства, отсутствием разрезов, формирования рубца и деформации контуров МЖ в послеоперационном периоде. Применение местной анестезии, возможность интраоперационной УЗ- и послеоперационной динамической МРТ-визуализации наделяет ЧК неоспоримыми преимуществами перед другими видами лечения.
Список литературы Вы можете найти на сайте http://www.rmj.ru
Источник: https://MedBlog.su/prochie-tematiki/chreskozhnaya-krioablyatsiya-fibroadenomy-molochnoj-zhelezy-shachinov-e-g-balahnin-p-v-shmelev-a-s-malkevich-v-i-bit-sava-e-m-egorenkov-v-v-moiseenko-v-m.html
Криоабляция раковых опухолей во Франции ✅
Уже даже смешно говорить о том, что рак не является смертельной болезнью. В арсенале французских онкологов целый ряд методик направленных на борьбу с этим недугом.
Начиная от нового поколения химиотерапии, которая является достаточно щадящей, химиотерапии в таблетках, что позволяет проводить лечение дистанционно и заканчивая супер точной 3д радиотерапией.
Также не стоит забывать о том, при некоторых видах рака очень хорошо себя проявила иммунотерапия.
Не стоит ждать – лечение онкологии важно!
Уже не для кого не секрет, что рак лучше всего поддается лечению на первой и второй стадия, однако, очень часто его диагностируют достаточно поздно, что несомненно является определённой сложностью даже для самых квалифицированных специалистов.
В наших статьях мы неустанно говорим о важности регулярного медицинского обследования, которым не стоит пренебрегать, ведь недаром именно рак называют молчаливым убийцей, ведь на первых стадиях заболевание происходит практически без единого симптома, а если они и есть, то на них мало кто обращает внимание.
Тот факт, что во Франции уровень смертности от рака является одним из самых низких в мире заслуга не только высококвалифицированных специалистов и новейших методик лечения, которые внедряются с завидной регулярностью, но и в техниках диагностики, в области которой Франция не раз отличилась.
Что же такое криоабляция в онкологии?
На сегодняшний день, в большинстве стран, одна из ведущих методик лечения рака это банальная операция. Она эффективна тем, что человек, у которого локализованное злокачественное образование, выходит из клиники абсолютно здоровым, так как во время операции все нездоровые ткани удаляются.
Проблема заключается в том, что обычно такие операции, как и любые серьёзные операции в принципе, требуют длительной госпитализации и долгого восстановительного периода.
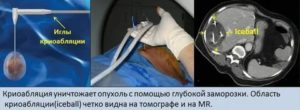
Криоабляция — это тоже самое удаление опухоли только при помощи холода, а именно заморозки пораженного опухолью участка. Таким образом криоабляция становится не просто безболезненным, легко переносимым методом лечения, но и …экономичным, ведь такая операция проводится амбулаторно и пациент не нуждается в госпитализации.
Как происходит криоабляция?
Для начала проводятся анализы для четкой локализации опухоли, затем доктор при помощи игл вводит специальных газ в область опухоли, который её замораживает и разрушает. Стоит отметить, что при проведении такой операции пациент не теряет ни грамма крови.
Первым, такую операцию в Париже произвел доктор де Кервиль, он вылечил за один день пожилого пациента от рака почек, превратив опухоль в кусок льда. Операция проходит в несколько этапов, так как для эффективной заморозки опухоль необходимо предварительно наполнить водой. Общая длительность операции около 30 минут.
Такое лечение проводится во Франции с 2008 года, однако, оснащение необходимым оборудованием все клиники и госпитали заняло немного времени.
Стоит отметить, что французы ждали больше 7 лет, чтобы данная методика подтвердила свою эффективность, так как консервативные французы относятся с презрением ко всем сомнительным инновациям о которых то и дело трезвонят то в одной то другой стране. Последствия не подтвердивших свою эффективность инноваций зачастую могут стать плачевными и подтверждений тому хоть отбавляй!
Преимущества метода – криоабляции
Криоабляция – минимально инвазивный метод, который не требует долгого восстановления пациента после процедуры. В этом основное преимущество подобного удаления поврежденных клеток. Однако это далеко не единственный фактор, который склоняет чашу весов в пользу заморозки. К другим преимуществам метода можно отнести:
- Воздействие низкими температурами исключает трофику (питание) патологических участков. Этот эффект достигается за счет того, что близко расположенные сосуды замерзают.
- Не всегда требуется хирургическое вмешательство – незначительные по величине опухоли рассасываются самостоятельно, удалять их нет необходимости.
- Метод отличается безболезненностью, а наркоз потребуется лишь в случае, когда предстоит работа с внутренними органами. Для большинства процедур достаточно местной анестезии.
- Стоимость процедуры значительно ниже, чем проведение операции.
- У метода гораздо меньше побочных действий по сравнению с другими способами удаления злокачественных образований.
- Криоабляция – это минимальные рубцы, что особенно важно для женщин.
Криотерапия относится к одному из наиболее лояльных методов удаления онкологии. Метод не имеет противопоказаний, а риски пациента минимальны. Однако в любом случае, всё зависит от конкретной ситуации, поэтому принять решение об эффективности заморозки под силу только опытному специалисту на основании полученных результатов диагностики.
Когда применяется криоабляция
Метод эффективен в ряде случаев, когда требуется удалить:
— различные образования на коже. Это могут быть как простые веснушки, так и серьёзные опухоли;
— поврежденные клетки в простате, печени, сердце, шейки матки;
— ретинобластомы.
Применяется заморозка и для удаления раковых опухолей в других органах, таких как: почки, кости, лёгкие, молочная железа.
Процедура в любом случае неизменна, меняется лишь температура и продолжительность воздействия. В редких случаях требуется дополнительное оборудование или разрезы тканей.
Чаще всего применяется криоабляция в тех случаях, когда более радикальные методы недопустимы или размер опухоли незначителен. Метод показывает хорошие результаты. Пациенты, прошедшие криоабляцию, уже через пару часов могут быть выписаны, однако для полного восстановления необходимо избегать поднятия тяжестей в течение 30 дней.За восемь лет развития метода, в 2010 году, практикующим врачам удалось достигнуть значительных показателей: применяя заморозку для удаления опухолей, локализованных в почках, частоту рецидивов снизили на 14%.
Возможные риски при проведении операции
Как и любой другой метод лечения, криоабляция имеет ряд рисков, которые в большинстве случаев определяются индивидуальной реакцией конкретного пациента.
Крайне редко укол сопровождается кровотечением, которое может возникнуть как снаружи, в месте прокола кожи, так и внутри, в органе, подвергшемся обработке.
Обращение к врачам низкой квалификации чревато тем, что могут быть задеты расположенные вблизи здоровые органы. Опытный врач всегда ориентируется на показания МРТ, компьютерной томографии и УЗИ, корректируя вхождение криозонда по полученным данным.
Проведение процедуры требует анестезии, что в некоторых случаях может вызвать нежелательные реакции у пациента.
Особенно велики риски при криоабляции простаты. Заморозка может привести к импотенции, шелушению слизистого слоя уретры, зажатию уретрального катетера. Большинство возможных осложнений связано с процессом работы специалиста, поэтому важно оказаться в надёжных руках.
Источник: https://www.MedifranceSolution.com/ru/news/krioablyaciya-rakovyh-opuholei-vo-francii-ili-kak-vylechit-rak-za-odin-den/
Методы лечения фиброаденомы молочной железы
Тактика лечения зависит от характеристик фиброаденомы и возраста пациентки. При опухоли небольшого размера (до 8-9 мм) девушки или женщины находятся под пристальным наблюдением врачей и 1 раз в несколько месяцев проходят процедуру УЗИ молочной железы.
Консервативная терапия включает контроль над динамикой течения болезни, коррекцию гормонального фона, устранение гинекологических проблем и лечение сопутствующих заболеваний.
Но как показывает практика, даже при комплексном консервативном подходе фиброаденома молочной железы рассасывается крайне редко.
Показания к оперативному вмешательству: прогрессивный рост фиброаденомы филлоидного типа (до 4-5 см за несколько месяцев), планирование беременности, физический и психологический дискомфорт, вызванный косметическим дефектом (деформацией молочной железы) при крупных опухолях. Хирургическое лечение проводится под местным или общим наркозом с помощью таких методов:
- Секторальное удаление — иссечение опухолевого образования вместе с окружающими тканями молочной железы с захватом от 1 см. Проводится в случае подозрений на озлокачествление фиброаденомы.
- Энуклеация — малоинвазивное лапароскопическое вылущивание опухоли, исключающее постоперационные осложнения. После энуклеации проводят гистологический анализ удаленных тканей.
За счет качественных разрезов и наложения подкожных швов, хирурги достигают хорошего косметического эффекта. Операция противопоказана при тяжелых заболеваниях крови, почек, сердечнососудистой и дыхательной системы.
Лазерная абляция — безопасное лечение фиброаденомы размером до 3 см с помощью лазера, который разрушает уплотнение без изменений формы молочной железы. Процедура проводится под местной анестезией и не требует реабилитации. После лазерной абляции на месте устраненной опухоли спустя 60-80 дней восстанавливается соединительная ткань.
Криоабляция — высокоточное замораживание фиброаденомы низкотемпературным жидким азотом через прокол криозонда под ультразвуковым контролем. Метод используется при множественных или единичных образованиях диаметром до 3,5-4 см.
Радиоволны — редко применяемая методика лечения, эффективная на ранней стадии патологии. В процессе радиоволновой операции рассекают ткани и уничтожают опухолевые клетки направленным высокочастотным радиоизлучением.
Маммотомическая биопсия — миниинвазивное удаление фиброаденомы. Во время процедуры используют биопсийный зонд, через который вакуумом эвакуируют пораженные ткани молочной железы.
